A excepción de los gases nobles, los átomos de la mayoría de los elementos son inestables en condiciones normales. Para que se estabilicen, ganan o pierden uno o más electrones de valencia y se convierten en iones. La ganancia o pérdida le da a los iones una carga positiva o negativa. Los iones con una carga positiva neta se llaman cationes mientras que aquellos con carga neta negativa son aniones. Estas cargas opuestas, también llamadas atracción electrostática, a menudo resultan en enlaces iónicos entre los átomos o moléculas. Un superíndice "-" es el signo utilizado después de la fórmula química para indicar cargas negativas, mientras que el superíndice "+" es el símbolo utilizado en la fórmula química para mostrar una carga positiva. Ejemplos de estas indicaciones son amonio (NH4 +), plata (Ag +), sulfato (SO42-) e hidróxido (OH-). Un ejemplo de un enlace iónico entre el potasio (K +) y el cloro (Cl-) es el cloruro de potasio (KCl).
¿Qué determina la pérdida o ganancia de electrones?
Según la posición de los elementos en la Tabla Periódica, los metales alcalinos y alcalinos en la mayoría de los casos forman cationes. Por otro lado, los halógenos y muchos otros elementos no metálicos forman aniones. Los metales alcalinos pierden un electrón, los metales alcalinos pierden dos electrones, y el aluminio y otros tres elementos del grupo pierden tres electrones. Por el contrario, los halógenos ganan un electrón; los elementos del grupo 6A ganan dos electrones mientras que los elementos del grupo 5A ganan tres electrones. O bien uno o varios átomos y moléculas pueden formar un anión. Si el anión está formado por un átomo, se llama anión monoatómico. Sin embargo, cuando está formado por dos o más átomos o moléculas, entonces es un anión poliatómico. La pérdida de uno, dos o tres electrones conduce a la formación de cationes monovalentes, divalentes y trivalentes, respectivamente.
Diferencias entre un catión y un anión
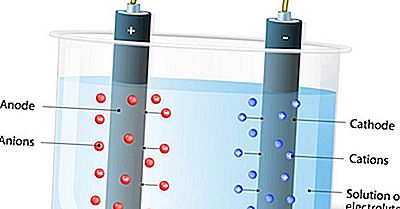
La primera diferencia es que los aniones poseen cargas eléctricas negativas, mientras que los cationes tienen cargas eléctricas positivas. En segundo lugar, durante la electrólisis, los aniones se mueven al electrodo positivo que se conoce como el ánodo. Sin embargo, los cationes migran al electrodo negativo llamado cátodo. Otra diferencia entre los dos iones es que los aniones tienen más electrones que protones, mientras que los cationes tienen más protones que electrones. Luego está la diferencia que se debe a la etimología de las palabras. Anión proviene de la palabra griega "ano" que significa "arriba". Por el contrario, el catión deriva su significado de una palabra griega "kata" que significa "abajo". Finalmente, los aniones son no metales mientras que los cationes son metales.
Aplicación del concepto de aniones y cationes
Los iones conducen la electricidad a través de líquidos o soluciones. Por lo tanto, los aniones y cationes son responsables del fenómeno del flujo de corriente eléctrica en una celda seca. La corriente siempre fluirá hacia la dirección de la carga positiva. Por otro lado, se mueve en la dirección opuesta al flujo de los portadores de carga negativa. En una celda seca, la electricidad fluye fuera del cátodo y fluye hacia el ánodo. El cátodo está cargado negativamente, atrayendo cargas positivas. Por otro lado, el ánodo está cargado positivamente, sacando solo la carga negativa.








